Hemostasia Secundária: Modelos de Cascata e da Superfície Celular
A hemostasia secundária é a fase crucial em que o tampão plaquetário inicial é consolidado pela deposição de fibrina, formando um coágulo estável e duradouro.
Tradicionalmente, esse processo é descrito pela cascata da coagulação, um modelo linear que detalha a ativação sequencial de fatores plasmáticos. Contudo, o modelo de superfície celular oferece uma perspectiva mais abrangente e fisiologicamente relevante, reconhecendo o papel fundamental das superfícies celulares ativadas na regulação espacial e temporal da coagulação.
Assim, a correlação desses dois modelos é essencial para a compreensão aprofundada da hemostasia e para enfrentar os desafios diagnósticos e terapêuticos em distúrbios da coagulação.
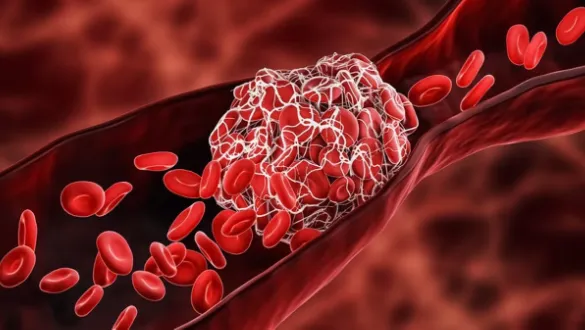
Imagem 1. Hemostasia. Fonte: https://www.lanacion.com.py
Hemostasia Secundária: Ativação da Coagulação Da Cascata aos Papéis Celulares
Nesse sentido, o modelo da cascata, a ativação ocorre por duas vias principais que convergem: a via extrínseca e a via intrínseca.
Via Extrínseca (Iniciação): Rapidamente ativada pela exposição do Fator Tecidual (FT), uma glicoproteína transmembrana presente em células subendoteliais e fibroblastos, após lesão vascular. Além disso, O FT se liga ao Fator VIIa circulante, formando o complexo FT-VIIa. Assim, este complexo é o principal iniciador da coagulação in vivo, ativando o Fator X e, em menor grau, o Fator IX. Esta é a fase de iniciação no modelo de superfície celular, ocorrendo em células que expressam FT.
Via Intrínseca (Amplificação): Ativada pelo contato com superfícies carregadas negativamente, como colágeno subendotelial. Envolve os Fatores XII, XI e IX. O Fator IXa, em conjunto com o Fator VIIIa (ativado pela trombina ou Fator Xa), forma o complexo tenase intrínseco, que ativa o Fator X de forma mais eficiente. No modelo de superfície celular, essa via é crucial na fase de amplificação, onde a trombina gerada inicialmente ativa cofatores e fatores, permitindo a formação de grandes quantidades de Fator Xa e, consequentemente, trombina nas superfícies plaquetárias.
Nesse sentido, a ativação do Fator X por ambas as vias culmina na via comum, onde o Fator Xa e o Fator Va (ativado pela trombina) formam o complexo protrombinase. Assim, este complexo, essencialmente na superfície de plaquetas ativadas, converte a protrombina (Fator II) em trombina (FIIa).
Hemostasia Secundária: Modelo De Superfície Celular
Desse modo, o modelo de superfície celular descreve a coagulação em três fases interligadas que ocorrem em diferentes superfícies:
- Iniciação: Em células que expressam FT (e.g., fibroblastos na lesão vascular), o complexo FT-VIIa gera pequenas quantidades de trombina.
- Amplificação: A trombina gerada na iniciação ativa plaquetas e cofatores (V, VIII, XI) plasmáticos. As plaquetas ativadas fornecem uma superfície fosfolipídica negativa crucial para a ligação e montagem dos complexos de coagulação.
- Propagação: Nas superfícies das plaquetas ativadas, os complexos tenase intrínseco e protrombinase são formados e operam de forma eficiente, levando a uma explosão de geração de trombina, garantindo a formação robusta de fibrina.
O Papel Central da Trombina e Seus Desafios de Avaliação da Hemostasia Secundária
A trombina é a protease central da hemostasia, desempenhando múltiplos papéis:
- Converte fibrinogênio em fibrina.
- Ativa os cofatores V e VIII e o Fator XI, amplificando a própria geração de trombina (feedback positivo).
- Ativa o Fator XIII, que estabiliza a rede de fibrina por ligações cruzadas.
- Promove a ativação e agregação plaquetária, reforçando o tampão.
Com isso, este papel multifacetado da trombina, especialmente seu feedback positivo, é um desafio para a avaliação laboratorial. Testes de coagulação padrão, como o Tempo de Protrombina (TP) e o Tempo de Tromboplastina Parcial Ativada (TTPA), avaliam o tempo necessário para a formação do coágulo, mas não refletem a quantidade e a cinética da geração de trombina.
Ademais, a Trombografia de Geração de Trombina (TGT) é uma ferramenta mais avançada que mede a formação de trombina em tempo real, fornecendo informações sobre o pico de trombina, o tempo para o pico e a quantidade total de trombina gerada, oferecendo uma visão mais completa da capacidade hemostática.

Regulação da Hemostasia Secundária e Implicações Clínicas
Nesse sentido, a regulação precisa da hemostasia é vital para prevenir tanto sangramentos quanto tromboses. Ademais, os mecanismos reguladores, como a antitrombina, o sistema proteína C (ativada pela trombomodulina na superfície endotelial) e o inibidor da via do fator tecidual (TFPI), limitam a coagulação ao local da lesão.
Desafios laboratoriais e clínicos surgem quando esses mecanismos estão desregulados:
- Monitoramento de terapia anticoagulante: O entendimento dos modelos de coagulação é fundamental para o monitoramento de anticoagulantes, como a heparina (que potencializa a antitrombina) e os novos anticoagulantes orais (que inibem fatores específicos como Xa ou trombina). Com isso, a precisão do monitoramento é crítica para otimizar a eficácia e segurança do tratamento.
- Deficiências de fatores da cascata: Como na hemofilia A (deficiência de FVIII) e B (deficiência de FIX), que resultam em sangramentos prolongados. O diagnóstico envolve a dosagem específica dos fatores. Dessa forma, o tratamento exige a reposição dos fatores deficientes, e a monitorização é feita pelos testes TP e TTPA, além da avaliação da geração de trombina para otimizar a dosagem.
- Estados de hipercoagulabilidade: Podem ser causados por deficiências de inibidores naturais (antitrombina, proteína C, proteína S) ou mutações que tornam os fatores mais resistentes à inativação (e.g., Fator V Leiden). Nesses casos, o risco de trombose aumenta, e o diagnóstico laboratorial envolve testes genéticos, dosagem de inibidores e, potencialmente, ensaios de trombofilia. Por isso, a interpretação desses testes é complexa, exigindo correlação com o quadro clínico e histórico familiar do paciente.
Conclusão
Portanto, a compreensão da hemostasia secundária, através da correlação dos modelos de cascata e de superfície celular, é indispensável para o diagnóstico e manejo de coagulopatias. Assim, o modelo de superfície celular, em particular, destaca a importância do microambiente celular na regulação espacial e temporal da formação do coágulo, o que tem profundas implicações para o desenvolvimento de terapias-alvo.
Logo, os desafios laboratoriais residem na capacidade de medir com precisão a dinâmica da coagulação e a função dos componentes celulares, enquanto os desafios clínicos envolvem a interpretação desses resultados complexos para um tratamento personalizado e eficaz. Por fim, a contínua pesquisa e o aprimoramento das técnicas de análise laboratorial são essenciais para avançar na prevenção e tratamento das desordens hemorrágicas e trombóticas.
Pós-Graduação em Hemostasia e Coagulação Sanguínea: Explore Novos Horizontes na Sua Carreira
Se você é um profissional dedicado na área da saúde em busca de aprimoramento e deseja desenvolver habilidades especializadas, senso crítico e expertise em Hemostasia e Coagulação, apresentamos a nossa Pós-Graduação como a escolha ideal para impulsionar sua carreira.
Desenvolvido meticulosamente para capacitar e atualizar profissionais como você, nosso programa altamente especializado oferece conhecimentos avançados que não apenas enriquecerão sua base de habilidades, mas também o destacarão no competitivo cenário profissional.
Oferecemos uma opção conveniente para quem busca uma pós-graduação 100% online e ao vivo, sem comprometer a excelência no ensino.
Nossa metodologia integra teoria e prática da rotina laboratorial, assegurando um aprendizado efetivo e aplicável.
Contamos com um corpo docente altamente qualificado, composto pelos melhores professores do Brasil, verdadeiras referências em suas respectivas áreas de atuação.
No Instituto Nacional de Medicina Laboratorial, nosso compromisso é singular: mais do que apenas transmitir conhecimento, buscamos transformar VOCÊ em uma referência.
Toque no botão abaixo e descubra mais sobre a Pós-Graduação em Hemostasia e Coagulação Sanguínea
Sua jornada de excelência começa aqui.
QUERO CONHECER TODOS OS DETALHES DA PÓS-GRADUAÇÃO
Referências:
BRASIL. Ministério da Saúde. Manual de diagnóstico e tratamento de inibidor em pacientes com hemofilia congênita. 2. ed. Brasília, DF: Ministério da Saúde, 2022.
BRASIL. Ministério da Saúde. Manual de diagnóstico laboratorial das coagulopatias hereditárias e plaquetopatias. Brasília, DF: Ministério da Saúde, 2016. Disponível em: http://bvsms.saude.gov.br/bvs/publicacoes/manual_diagnostico_coagulopatias_hereditarias_plaqueopatias.pdf. Acesso em: 26 jun. 2025.
MICHELSON, A. D. (ed.). Platelets. 3. ed. San Diego: Academic Press, 2013. ISBN 9780123878373.SOTO ORTEGA, I.; ÁLVAREZ ROMÁN, M. T. (ed.). Hemostasia y trombosis en la práctica clínica. 2. ed. Madrid: Ergon, 2024. ISBN 978-84-19955-44-9.